合金|初中化学金属部分15个重要考点总结( 三 )
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
金属活动性:由强到弱
【合金|初中化学金属部分15个重要考点总结】应用:在金属活动性顺序里 , 金属的位置越靠前 , 它的活动性越强 。
(1) 在金属活动性顺序里 , 位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸) 。
(2) 在金属活动性顺序里 , 位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来(K、Ca、Na除外) 。
考点11
矿石
1. 金属资源的存在方式:地球上的金属资源广泛存在于地壳和海洋中 , 大多数金属化合物性质较活泼 , 所以它们以化合物的形式存在;只有少数金属化学性质很不活泼 , 如金、银等以单质形式存在 。
2. 矿石:工业上把能提炼金属的矿物叫矿石 。
3. 常见矿石名称与其主要成分:
考点12
一氧化碳还原氧化铁
(1)仪器:铁架台(2个)、硬质玻璃管、单孔橡皮赛(2个)、酒精灯、试管、酒精喷灯、双孔橡皮赛、导气管 。
(2)药品:氧化铁粉末、澄清石灰水、一氧化碳气体
(3)装置图:
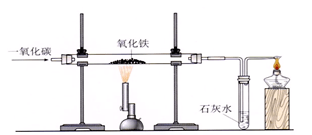
文章图片
(4)步骤:①检验装置的气密性;②装入药品并固定;③向玻璃管内通入一氧化碳气体;④给氧化铁加热;⑤停止加热;⑥停止通入一氧化碳
(5)现象:红色粉末逐渐变成黑色 , 澄清石灰水变浑浊 , 尾气燃烧产生蓝色火焰 。
(6) 化学方程式:
3CO+Fe2O3==高温==2Fe+3CO2
2CO+O2==点燃===2CO2
Ca(OH)2+CO2=====CaCO3↓+H2O
(7) 注意事项:要先通入CO再加热 , 实验完毕 , 停止加热 , 继续通入CO至试管冷却 。
(8) 尾气处理:因CO有毒 , 不能随意排放在空气中 , 处理的原则是将CO燃烧掉转化为无毒的CO2或收集备用 。
考点13
工业炼铁
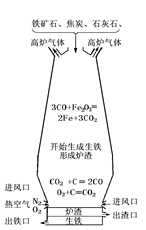
文章图片
(1)原理:在高温下 , 利用焦炭与氧气反应生成的还原剂(CO)将铁从铁矿石里还原出来 。
(2)原料:铁矿石:选择矿石条件常见的铁矿石有磁铁矿(主要成分是Fe3O4 )、赤铁矿(主要成分是Fe2O3 )
焦炭作用:(1)提供高温 C+O2==高温==CO2
(2)提供CO CO2+C==高温==2CO
石灰石:作用除去SiO2
CaCO3==高温===CaO+CO2↑
CaO+SiO2==高温===CaSiO3
(3)主要设备:高炉
(4) 冶炼过程中发生的化学反应:
C+O2==点燃==CO2
CO2+C==高温==2CO
3CO+Fe2O3==高温==2Fe+3CO2
CaCO3==高温===CaO+CO2↑
CaO+SiO2==高温===CaSiO3
注意:石灰石的主要作用是将矿石中的二氧化硅转变为炉渣 。
推荐阅读
- 恐龙|广东一地,首次发现恐龙足迹!系初中生偶然发现
- 基合金|兰石重装研制国产化N08810换热器完工交付
- 线性|微星推出 MSI GK71 Sonic 电竞机械键盘:自研线性轴,铝合金底壳
- IT之家|微星推出MSI GK71 Sonic电竞机械键盘:自研线性轴,铝合金底壳
- IT|眼镜防雾剂/防雾擦中发现高含量的潜在有害PFAS化学品
- 收音机|组装半导体
- 水杨|万物可变化,化学真奇妙
- 股份|永福股份设计的国内首个220kV铝合金干字型塔通过真型试验
- 生物化学|我国卓越科技论文总体产出持续增长
- 生物地球化学过程|我国科学家发现第五条甲烷产生途径






