细胞协同迁移在多种生理和病理过程中都至关重要 , 例如生命体的形态发生、伤口愈合、癌症侵袭和免疫反应 。 在协同迁移过程中 , 细胞是如何进行通讯的也是一直以来备受关注的问题 。 近几十年来 , 研究发现细胞外基质 (Extracellular matrix, ECM) 不仅为细胞迁移提供了支架 , 也为细胞间机械信号的传递提供了介质 。
在迁移过程中 , 单个细胞可以通过胞内肌动蛋白收缩产生主动拉力 , 进而通过粘着斑复合物施加到 ECM 上 , 使 ECM 变形重构 。 I型胶原蛋白(Collagen I)是体内最丰富的 ECM 成分 , 并有着特定的非线性粘弹性和纤维状微结构 。 目前已有多个实验及模拟研究工作证明Collagen纤维束结构可以辅助长距离的细胞间力学信号传递 。 然而 , 目前仍然缺乏直接的实验证据来验证细胞之间重组的胶原纤维束是否确实携带弹性力/张力 , 以及它们是如何引导细胞迁移并诱导细胞运动的长程相关性 。
中国科学院物理研究所/北京凝聚态物理国家研究中心软物质实验室SM4组的叶方富研究员、樊琪慧副研究员和亚利桑那州立大学焦阳教授、南京大学鼓楼医院赵远锦教授合作 , 利用具有可调刚度的纤维状天然水凝胶Collagen构建了一个准三维系统 , 将上皮细胞接种在胶原蛋白水凝胶和培养基之间的界面上 , 用于模拟细胞在体内微环境中的状态 。 在该三维微环境中 , 细胞通过动态重构Collagen纤维束形成连接 , 并且相互连接的细胞对之间有很强的相向运动 。 在有效范围内 , 多个互不接触的离散细胞间通过动态重构的Collagen纤维束可以发生远程关联并形成多体运动的强相关网络 。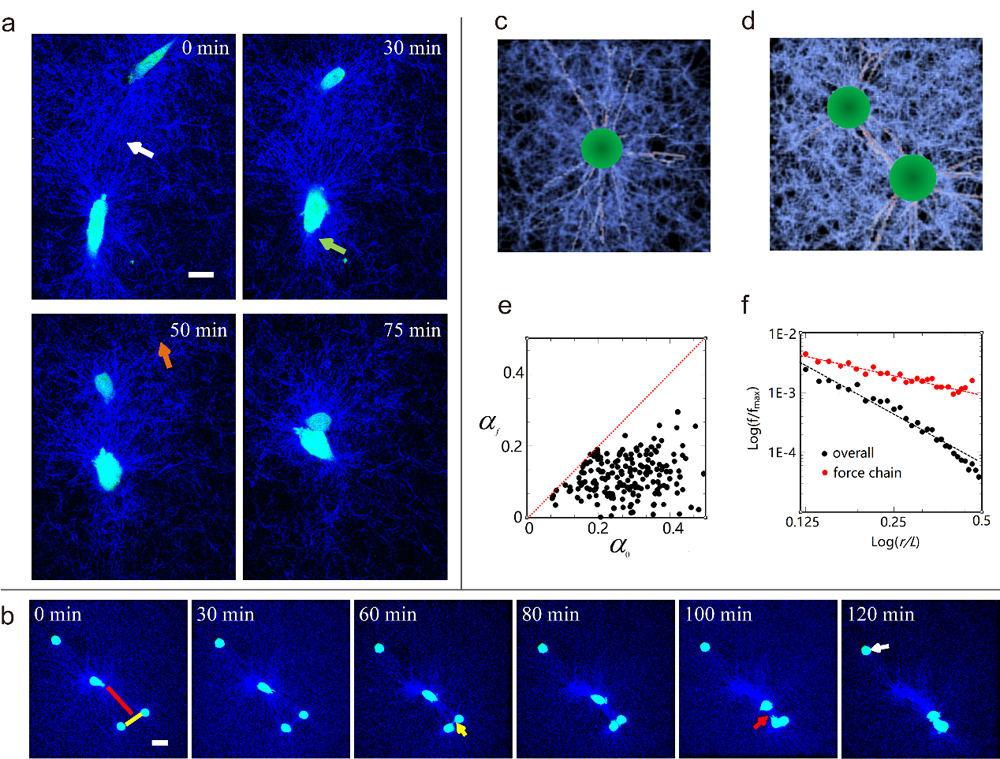
本文图片
图1. (a)在三维微环境中 , 通过Collagen纤维束所连接的细胞对之间有很强的吸引作用 , 导致细胞间可以进行快速持续的相向运动;(b)在有效范围内 , 多个离散细胞间通过动态重构的Collagen纤维束发生远程关联并形成多体运动的强相关网络;(c-f)理论模型可以很好模拟和重现三维微环境中细胞间的强关联作用 。
研究还将飞秒激光显微切割技术整合到 3D 实时跟踪系统中 , 证明了细胞间动态重构的Collagen纤维束中确实存在张力 , 并且细胞间的动力学强关联是由张力、而不是纤维束的有序几何微结构导致的 。 一旦细胞间纤维束被激光切断 , 或通过抑制肌球蛋白降低细胞收缩力 , 细胞之间运动的强关联性就消失了 。 这些研究结果提供了最为直接的实验证据 , 证明通过Collagen纤维束所传递的力学信号对于细胞迁移的远程通讯至关重要 。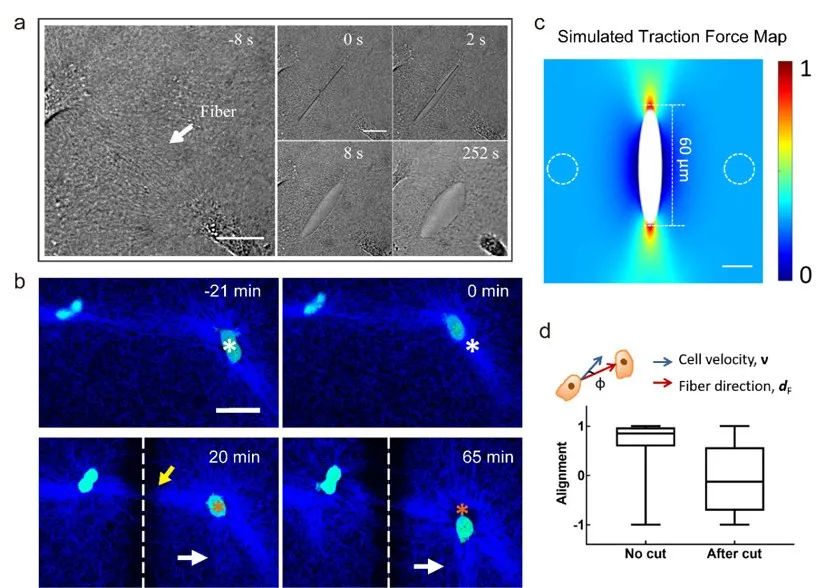
推荐阅读
- 技术|“2”类医械有重大进展:神经介入产品井喷、基因测序弯道超车
- 重大进展|“2”类医械有重大进展:神经介入产品井喷、基因测序弯道超车
- 建设|5G信号全覆盖,冬奥会各赛区通信基础设施建设全部完成
- 商家|重磅!微信支付全面开放,互联互通进展神速
- 最新消息|欧拉好猫“芯片门”最新进展:赔偿车主1万现金
- 地铁|信号女子突击队:巧手“绣”出铁路“神经网”
- 视点·观察|课外体育培训行为“规范”释放了什么信号?
- 产品|国产半导体新进展 展锐第二代5G芯片平台实现客户产品量产
- 数据|信号源的 10 种常见测试应用的讲解
- 量子|美国《信号》杂志预测2022年十大技术趋势





