【TwinF|《科学》:新型抑制剂有望治疗神经退行性疾病】原创 图图 神经现实
文章图片
文献:Yan, Jing, et al. "Coupling of NMDA receptors and TRPM4 guides discovery of unconventional neuroprotectants." Science 370.6513 (2020).
DOI:https://doi.org/10.1126/science.aay3302
导读作者:图图 | 封面:Curtis Cripe
N-甲基-D-天门冬胺酸受体(N-methyl-D-aspartate receptor , NMDAR)是众所周知的离子型谷氨酸受体 , 可介导钠离子、钙离子等的跨膜运输 。 他们不仅对大脑的发育及突触可塑性调节至关重要 , 对记忆及获得性神经保护等适应性机制的加固也是必不可少的 。
然而 , 天使与恶魔同在 , NMDAR也有着鲜为人知的黑暗面-中断遗传物质转录、导致线粒体罢工 , 更甚能引起兴奋性神经元中毒及死亡 。 直到如今 , 我们也并不清楚他是如何在这两种“人格”中游走 , 为何他会对一心要保护的神经元下此毒手?

文章图片
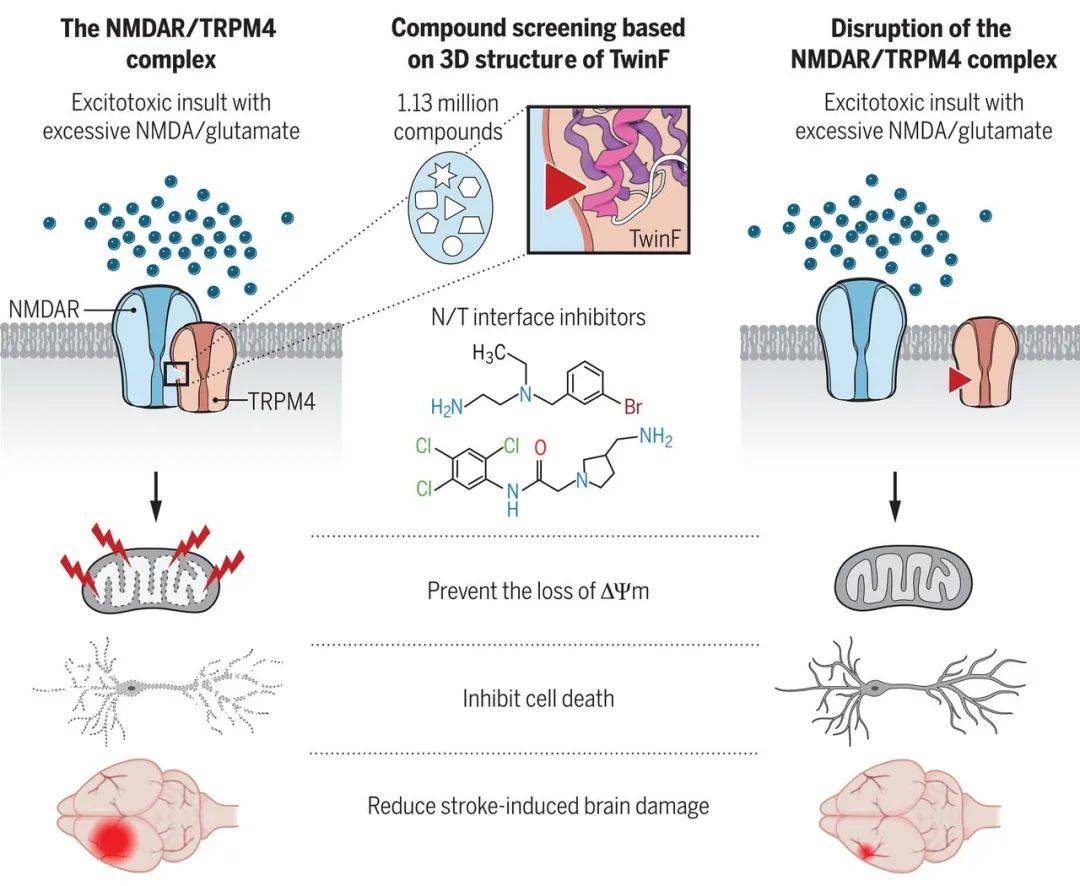
近日来自德国海德堡大学的科学家们在Science杂志上发表了他们的研究 , 他们致力于寻找NMDAR与细胞凋亡之间的结构基础 , 发现NMDAR获得毒物的特质是因为与瞬态感受器电位阳离子通道子类M的4号成员(TRPM4)之间发生相互作用形成复合体 , 而并不是大众之前所认为的细胞内高钙离子负荷 。 所以 , 他们猜想如果能破坏NMDAR/TRPM4 (N/T)之间的联系 , 也许能够消除NMDAR引起的细胞毒性减少神经元的伤亡 。
接下来 , 他们以结构为基础进行计算药物筛选 , 发现TRPM4细胞内结构域只有57个氨基酸的TwinF对N/T联系至关重要 , 无论表达TwinF或者利用基于TwinF结构筛选出的抑制剂小分子都可以在不破坏NMDAR和TRPM4离子通道的基础上 , 解除他们之间的关联 , 最终达到恢复遗传物质转录、线粒体正常工作等保护细胞的功效 。 这项新研究为一直以来很难有效治疗的神经退行性疾病提供了新的攻克方向 。
文章图片
- Yan et al., Science -
文章图片
阅读原文
推荐阅读
- 原神|《原神》「飞彩镌流年」2.4 版本预下载已开启
- 科学|中阳县北街小学:体验科学魅力
- 牛上|英媒文章:2021年最有趣的科学发现
- 核心|中科大陈秀雄团队成功证明凯勒几何两大核心猜想,研究登上《美国数学会杂志》
- 曹志兴|90后教授曹志兴:最一流的基础科学来源于好奇心
- 审判|直接服务“三城一区”主平台,怀柔科学城知识产权巡回审判庭成立
- 龙珠|realme GT2 Pro 预热,联名《龙珠》定制新品
- 短片|马蜂窝推全球首份《星际太空旅行指南》,发布年度短片
- 生物地球化学过程|我国科学家发现第五条甲烷产生途径
- 孩子|“双减”后 科学实践课如何做好“加法”







