IT 人-猴嵌合体:培育人类器官又向前跨越一小步
近日昆明理工大学和美国索尔克生物研究所的科学家团队在《细胞》杂志上发表论文,宣布成功构建了世界首例人-猴嵌合胚胎,即同时具有人和猴细胞来源的胚胎 。这一发现表明人源多能干细胞能够在猴子胚胎中存活并整合,并且有向不同器官类型分化的趋势 。
那么,这项研究的意义究竟是什么?是否能够为人类器官移植研究带来新的希望?又或是对科研伦理提出了新的的挑战?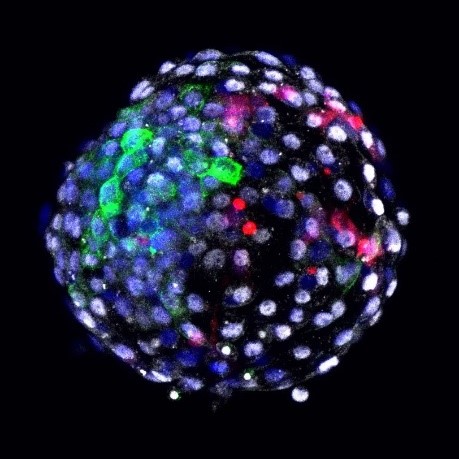
文章图片
器官移植面临的挑战
在器官移植技术得以临床运用之前,许多疾病,例如终末期肾功能衰竭,终末期肝硬化的病人可能只能在重症监护室中通过透析机等机器来维持生命,并最终死亡,给许多家庭带来了沉重的精神和经济负担 。随着器官移植技术的临床普及,给予了很多病人第二次生命,因此器官移植也被称为“二十一世纪医学之巅” 。1990年两名器官移植的先驱,美国医生Joseph Murray和EDonnall Thomas获得了诺贝尔生理和医学奖 。
【IT|人-猴嵌合体:培育人类器官又向前跨越一小步】然而,器官移植现状却是:全球每年大概有200万人亟待通过器官移植拯救生命,我国每年约有30万人需器官移植,最终只有约1万人能完成移植 。等待,焦急的等待,最终绝望的等待可能是绝大多数病人的现状,也是我们健康人无法体会到的痛楚 。此外,即便获得了可移植的器官,巨额的治疗费用以及随后长期服用抗排斥药物的费用,仍然是患者巨大的负担 。若能以患者自身来源的多能干细胞为材料,再利用实验动物产生出具有功能的器官移植回患者体内,就能有效避免排斥反应的发生,这必将是医学发展的又一高峰 。而嵌合体技术,就是实现这一设想的重要手段 。
异种嵌合体技术打开了器官供体来源的另一扇门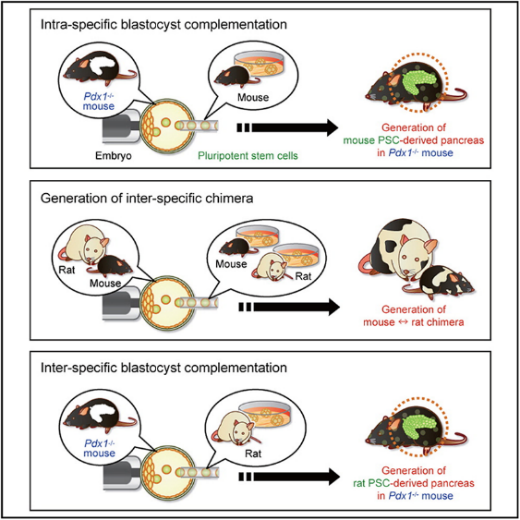
文章图片
2010年东京大学中内启光(Hiromitsu Nakauchi)团队在《Cell》发表研究成果,通过异种嵌合体技术,将大鼠的多能干细胞注射到不能形成胰腺的小鼠囊胚中,移植回代孕母鼠体内,产生了具有健康胰腺的小鼠 。但是该胰腺只有小鼠胰腺大小,分离出的胰岛数量太少而不能用于治疗糖尿病大鼠模型 。随后2017年该团队在《Nature》公布了研究成果,实现了在大鼠体内产生了完全来自于糖尿病小鼠多能干细胞的自体胰腺,分离出能正常分泌胰岛素的胰岛组织,并移植到患糖尿病的小鼠体内后,成功控制了小鼠的血糖水平 。这些研究成果令大家感到兴奋,异种嵌合体技术为器官的异种来源带了曙光 。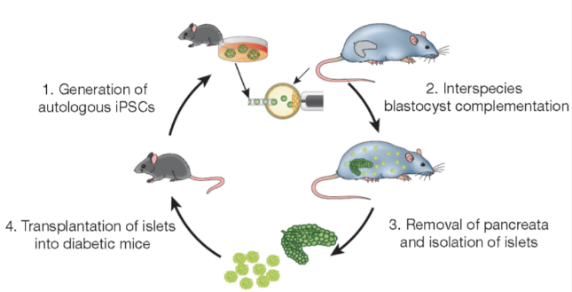
文章图片
1年后小鼠的血糖值依然维持在正常水平(Toshihiro Kobayashi et al,cell,2010; Toshihiro Kobayashi et al,nature,2017) 。
实现在动物体内培育出可供移植的人类器官还要多久?
虽然小鼠-大鼠异种嵌合的成功给人类利用异种嵌合技术获取人类器官带来了希望,但是要实现在动物体内培育出可供移植的人类器官还相当遥远!科学家希望有一天能够在猪的体内运用病人干细胞,生产所需器官,因为猪的肾脏,心脏,胰腺等器官,与人器官的大小接近,且用猪作为人器官生产的供体更容易被大众所接受 。为此,2017年科学家成功在猪体内成功培育出3到4周的人猪嵌合体(相当于人类怀孕8到10周),令人遗憾的是,这些猪的胚胎中,每十万个猪细胞中可能才只有一个人的细胞 。远远没有达到能够有效在体内产生功能性组织的水平 。要知道在进化距离较近的大鼠和小鼠之间,两者整体嵌合率可以达到20%-30% 。通过互补,在某些器官嵌合率可以达到90% 以上 。
文章图片
图来源于:https://www.utsouthwestern.edu/labs/wu-jun/contact/
为了提高嵌合效率,全球科学家做了很多努力,2017年通过在人类胚胎干细胞中过表达抗凋亡基因BCL2及BCL2L1,获得了人-鼠异种嵌合小鼠胚胎,并证明其同时具有胚内、胚外组织的嵌合能力 。在10.5天的人小鼠嵌合体中检测到人干细胞的嵌合率高达1% 。通过建立具有胚内和胚外发育潜能的小鼠和人的新型多能干细胞,即具有全能性特征的多潜能干细胞系(EPS细胞) 。并且证明人EPS细胞注射到早期小鼠胚胎后,能够稳定地嵌合到小鼠胚内和胚外组织中,其胚内整合比例比已报道的整合效率提高了近20倍 。2019 年我国科学家优化了嵌合体构建技术,实现了“猪猴嵌合体”,并存活1周 。嵌合体仔猪各个器官嵌合率在千分之一和万分之一之间,极大了提高了效率,异种嵌合向着临床运用又迈向了坚实的一步 。
推荐阅读
- 云南花25亿建“假古镇”,如今遭人“嫌弃”,当地人:不会再去
- 最新消息 麻省理工学院研发可编程数字纤维 有内存传感器和人工智能
- 哥伦比亚大学 人类是否能够再造个地球环境,进行移民,生物圈2号告诉我们还是洗洗睡吧
- 万人 罗志祥最新综艺节目暂时停播,因不到5万人观看,他凉了吗?
- 中国人 高晓松在晓松奇谈中言论引争议
- 停播 罗志祥的新综艺暂时停播,不到5万人观看,综艺效果很惨淡
- 爱迪生 杨振宁所不为人知的身份,足以跟爱因斯坦、爱迪生齐名!
- 电子商务 京东阿里美团为无人配送拼了:3年单车成本砍八成、投放或超万辆
- Apple iOS 14.7 Beta 2曝出“SIM卡失败”Bug 测试人员应避开该版本
- 摩托车 王一博,是铁了心要靠自己;而有的人,是铁了心要靠王一博!







